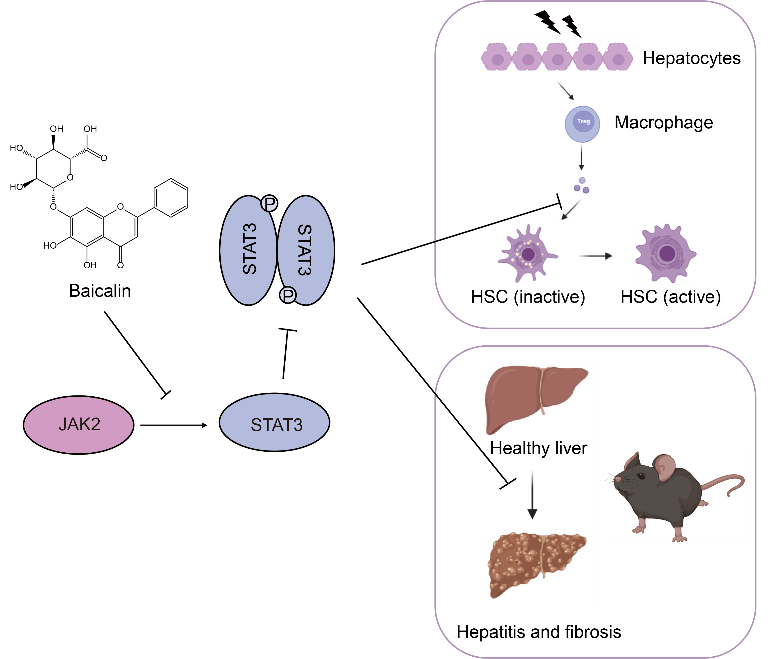
近日,太阳成集团tyc122ccvip、北大-清华生命科学联合中心、北大成都前沿交叉生物技术研究院王初课题组在National Science Review杂志发表题为“Chemoproteomics Identifies STAT3 as a Key Target of Baicalin in Ameliorating Liver Fibrosis”的研究论文。研究结合定量化学蛋白质组学与遗传学功能验证,鉴定并确立STAT3为黄芩苷发挥抗肝纤维化作用的关键直接靶点,并揭示黄芩苷通过阻断JAK2–STAT3信号轴抑制下游促纤维化反应的机制,为相关抗纤维化药物设计提供了靶点与机制依据。
肝纤维化是慢性肝损伤后异常修复导致的细胞外基质过度沉积,可进展为肝硬化甚至肝细胞癌,临床负担沉重。尽管大量候选药物进入临床研究,目前仍缺乏特异有效的抗肝纤维化药物。天然产物因结构多样、相容性良好而具有重要药源价值,但其转化常受限于靶点不清、机制不完整。此前,王初课题组曾利用定量化学蛋白质组学发现黄芩苷降脂作用的直接靶点CPT1A,并阐明其治疗肥胖及相关代谢疾病的分子机制(PNAS. 2018, 115, E5896–E5905)。该研究在既往黄芩苷抗纤维化活性报道基础上,系统鉴定其直接互作蛋白并锁定功能关键靶点。
为评估黄芩苷的治疗潜力,作者在四种不同病因机制的小鼠肝纤维化模型中进行药效学验证。结果显示,黄芩苷给药(100 mg/kg)可显著降低Masson染色评估的胶原沉积,并下调细胞外基质相关基因及肝星状细胞活化标志基因,提示其可能通过抑制肝星状细胞活化发挥较广谱的抗纤维化效应。以人肝星状细胞系LX-2为体外模型,作者进一步发现黄芩苷可剂量依赖性抑制TGFβ1诱导的SMAD3磷酸化及SMAD3响应型报告基因活性,表明其可干预关键促纤维化通路。
在靶点解析方面,作者设计并合成保持生物活性的黄芩苷光交联探针,并结合二甲基化定量化学蛋白质组学,在肝组织与LX-2细胞裂解液中鉴定到174个黄芩苷结合蛋白;随后按竞争比排序,筛选前15个候选靶点进入功能验证。在LX-2细胞中对候选蛋白开展敲低/敲除筛查结果显示,敲除STAT3可完全消除黄芩苷对SMAD3磷酸化的抑制作用,提示STAT3处于枢纽位置。进一步在小鼠体内构建肝特异Stat3 敲除模型,在DDC饮食诱导纤维化背景下,敲除Stat3 的小鼠对黄芩苷治疗呈“耐受”,胶原沉积及纤维化标志基因不再随给药显著下降。机制研究表明,黄芩苷主要结合STAT3的N端结构域,并抑制STAT3与上游激酶JAK2的相互作用,从而降低STAT3磷酸化并削弱下游信号输出。生物物理实验测定支持黄芩苷与STAT3 N端结构域直接结合。
综上,该研究以“定量化学蛋白质组学靶点解析 + 遗传学因果验证”的策略,明确STAT3是黄芩苷改善肝纤维化的关键靶点,为黄芩苷及其衍生物的结构优化与抗纤维化药物研发提供了理论基础,也为天然产物“靶点不明”问题提供了可推广的研究范式。
该文通讯作者为太阳成集团tyc122ccvip、北大-清华生命科学联合中心、北大成都前沿交叉生物技术研究院的王初教授。第一作者为王初课题组博士后袁守丽和周元飞以及博士研究生马斌。此外,王初课题组刘源副研究员,博士毕业生张锦,博士研究生王彦琦,北大成都前沿交叉生物技术研究院的肖伟弟博士、中国中医科学院杨伟鹏教授及团队成员刘海帆等人也为该课题做出了贡献。该工作得到了国家自然科学基金、科技部重点研发计划、北京分子科学国研中心创新研究团队、教育部学科突破先导等项目的支持。